Инсульт остается одной из основных причин инвалидизации взрослого населения по всему миру [1]. Ограничения уровня нормального функционирования и независимости пациентов закономерно отражается на качестве их жизни и является значимым экономическим бременем для системы здравоохранения. Именно поэтому во всем мире уделяется особое внимание как проблемам профилактики инсультов и своевременной тромболитической терапии, так и комплексной мультидисциплинарной реабилитации, начинающейся уже с палат интенсивной терапии в виде первого этапа реабилитации и продолжающейся дома на третьем этапе.
В данной ситуации специалисты, занимающиеся восстановительным лечением, сталкиваются с со сложностями определения реабилитационного потенциала пациента для его дальнейшей маршрутизации и прогноза восстановления [2]. На основании данной оценки строятся план и программа реабилитации, с обозначением рассчитываемых сроков для достижения тех или иных задач. Пациенты с высоким реабилитационным потенциалом особенно нуждаются в четкой последовательной программе, преемственной на всех этапах реабилитации, для реализации имеющихся возможностей. В то же время другая часть пациентов может быть быстрее перенаправлена в органы социальной защиты для обучения и адаптации к жизни с имеющимися ограничениями. В данных условиях меняется время нахождения пациента на том или ином этапе реабилитации, где особенно остро возникает вопрос третьего этапа реабилитации и поддержки пациента на дому. Согласно Приказу МЗ РФ от 29 декабря 2012 г. N 1705н, третий этап реабилитации должен реализовываться выездными бригадами на дому или в амбулаторных условиях при наличии перспективы на восстановление функций – реабилитационного потенциала. Если обратиться к опыту скандинавских стран, то амбулаторная реабилитация организована там как 45-минутные занятия лечебной гимнастикой в среднеинтенсивном режиме 1 раз в неделю в течение 3-6 месяцев после инсульта [3]. При этом обсуждается, что физическая активность должна носить ежедневный характер не менее 30 минут; препятствиями для обеспечения такого режима можно назвать сложности транспортировки пациентов, экономические затраты и низкую мотивацию, а также приверженность программе реабилитации. При анализе базы данных пациентов отделения реабилитации НМХЦ им. Н.И. Пирогова за последние 3 года было отмечено, что две трети пациентов после инсульта не продолжали амбулаторную реабилитацию по тем или иным причинам, и при повторных госпитализациях демонстрировали отсутствие прогресса, а иногда и регресс достигнутых реабилитационных результатов. При опросе более 300 пациентов удалось выделить две основные причины нынешнего положения дел: недостаток учреждений и специалистов амбулаторного этапа, гипомобильность пациентов в труднодоступной среде.
Таким образом, реалии таковы, что потребности пациентов в амбулаторных медицинских услугах во всем мире гораздо превышают имеющиеся ресурсы, что требует поисков альтернативных решений и подключения современных и передовых технологий для поддержки пациентов, как на третьем этапе реабилитации, так и в рамках программ по социальной защите населения. Одним из таких решений явились телекоммуникационные технологии, ставшие не только способом доставки реабилитационных программ пациенту, но способом контроля за их выполнением. Отсутствие единой методологии, способов лечебного воздействия и информационной платформы привело к созданию множества разноплановых приложений для телереабилитации с той или иной степенью эффективности, но чаще имеющих ограниченное применение по юридическим или экономическим причинам: защита персональных данных, стоимость самой программы, дополнительное оборудование, владение компьютером и т.д. Под домашней телереабилитацией в данной ситуации можно понимать метод реабилитации, когда специалисты используют устройства телекоммуникации (телефон, видеофон, аудио-видео конференц-связь) для предоставления методических рекомендаций, оценки динамики восстановления и поддержки пациентов на дому [4].
В НМХЦ им. Н.И. Пирогова активно исследуются и интегрируются новые технологические решения в рутинную клиническую практику, и метод телереабилитации не стал исключением. При участии сотрудников НМХЦ им. Н.И. Пирогова была разработана компьютерная программа «Степс-реабил», целью которой является предоставление пациентам информационного сопровождения на третьем этапе реабилитации и сохранение преемственности индивидуальной реабилитационной программы со стационарного на амбулаторный уровень. Данное программное обеспечение позволяет специалисту по двигательной реабилитации, наблюдающему пациента в стационаре, быстро составить индивидуальный комплекс ЛФК для самостоятельных занятий в видео-формате. Кроме того, данный комплекс корректируется каждые месяц в зависимости от динамики восстановления, что обеспечивает дополнительный контроль для пациента. Основной целью было разработать максимально простой и доступный для пациентов способ продолжать занятия лечебной гимнастикой на дому в индивидуальном режиме и под контролем специалистов. Технологическое решение позволяет использовать индивидуальную реабилитационную программу при минимальных параметрах производительности электронно-вычислительных машин и минимальном уровне пользования компьютером, также не требуется постоянной и быстрой интернет связи. Минимализм и простота с одной стороны, и огромная база отдельных упражнений ЛФК, нейропсихологических и логопедических заданий – с другой, позволяют создавать индивидуальные комплексы для пациентов практически любого социального статуса и места проживания с минимальными временными и трудозатратами для специалистов. При этом подразумевается, что у тяжелых пациентов есть ухаживающие, которые смогут ассистировать при выполнении упражнений, копируя четкие и ясные движения инструктора.
Для оценки перспектив применения данного подхода, реализованного в программе «Степс-Реабил», было начато многоцентровое проспектовое исследование. В данной статье представлены предварительные результаты рандомизированного простого предварительного исследования.
ЦЕЛЬ ИССЛЕДОВАНИЯ
Целью данного исследования было оценить эффективность амбулаторного видео сопровождения посредством программы «Степс-Реабил» на амбулаторном, третьем этапе реабилитации.
МАТЕРИАЛ И МЕТОДЫ
Пациенты, поступающие на восстановительное лечение в отделении медицинской реабилитации НМХЦ им. Н.И. Пирогова с мая по сентябрь 2018 года, были рандомизированы с помощью генератора случайных чисел (http://www.calculator888.ru/generator-sluchajnyh-chisel) в основную или контрольную группу.
Критерии включения:
- диагноз инсульта, верифицированный на КТ/МРТ; – возраст – от 40 до 80 лет; – пол – мужчины и женщины;
- период заболевания: подострый (от 3 недель до 3 месяцев) и ранний восстановительный (до 12 месяцев);
- тяжесть инсульта в острый период по шкале NIHSS (National Institutes of Health Stroke Scale) 9-15 (от средней до тяжелой);
- степень функционирования по модифицированной шкале Рэнкина (mRS) 4 и 5;
- монреальская шкала когнитивной оценки (MMSE) 20-27 баллов; – подписанное информированное согласие.
Критерии исключения:
- наличие у пациента грубых когнитивных нарушений или психических заболеваний, препятствующих правильному выполнению инструкций;
- тяжёлые кардиоваскулярные, печеночные, неврологические, эндокринологические и другие системные заболевания, препятствующие выполнению данного протокола и искажающие конечные результаты исследования или влекущие повышенный риск для пациента при условии участия в исследовании.
Протокол лечения
Второй этап реабилитации пациентов начинался в стационаре и продолжался 14 дней. Программа реабилитации включала в себя лечебную гимнастику, индивидуальную и роботизированную механотерапию, и индивидуальные занятия с нейропсихологом в графике 5/2. Назначаемые лекарственные препараты были сведены к минимуму: терапия артериальной гипертензии, сахарного диабета, мерцательной аритмии, гиперкоагуляции и гиперхолестеринемии. При выборе препарата внутри лекарственной группы предпочтение отдавалось одному и тому же препарату у всех испытуемых, если это не влекло ущерба для пациента. Выбор был обусловлен утвержденным списком лекарственных препаратов, применяемых внутри НМХЦ им. Н.И. Пирогова. Пациенты получали ежедневное внутривенное введение 30 мл церебролизина, растворенного в 200 мл физиологического раствора в непрозрачном флаконе в основной группе и 200 мл физиологического раствора в непрозрачном флаконе без активного препарата в контрольной в течение 30-40 минут (флаконы с вводимым раствором одинаковые во всех группах, скорость введение 2 капли в секунду). Церебролизин был использован в контрольной группе, как препарат, продемонстрировавший определенный потенциал в ускорении и улучшении восстановления двигательных функций после инсульта [5-7]. Вопрос влияния церебролизина на когнитивные функции, такие как память, внимание, пространственное ориентирование, требует дальнейшего изучения.
После стационарного лечения пациенты были выписаны на третий этап реабилитации. Лицам в обеих группах было рекомендовано продолжать занятия лечебной гимнастикой амбулаторно и самостоятельно выполнять упражнения по индивидуальной программе. Пациенты в основной группе имели возможность следовать индивидуальному плану реабилитации с помощью программы «Степс-Реабил» с коррекцией данного плана врачом ЛФК через 1 и 2 месяца после выписки. Пациенты в контрольной группе пользовались возможностями амбулаторной реабилитации в том виде, который она имела на тот момент, и были проинструктированы ежедневно заниматься самостоятельно. Оценка эффективности терапии проводилась по шкалам MoCA (Монреальская шкала когнитивной оценки), Оксфордского когнитивного скрининга (ОКС), mRS, ИМР на 1, 14,104 день. Оценка безопасности терапии оценивалась на основании активных жалоб пациента.
Статистический анализ
Статистическая обработка результатов осуществлялась с применением пакета анализа Microsoft Excel, а также при помощи пакета программ Statistica 6.0. Распределения количественных данных, отличные от нормального, описывали c указанием медианы (Ме) и интерквартильного размаха в виде 25-го и 75-го процентилей. Значимость различий оценивали по методу вариационной статистики с использованием критериев Манна-Уитни для независимых выборок и критерия Уилкоксона для парных случаев непараметрических распределений. Различия считали статистически значимыми при значениях p<0,05.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
В исследовании приняли участие 39 человек, которые случайным образом были распределены в основную и контрольные группы.
В основную группу изначально вошли 19 человек. В процессе исследования по причине обострения сопутствующей патологии двое пациентов (10,5%) не смогли продолжить своё участие. Таким образом, завершили исследование 17 человек (89,5%).
Среди них женщин было 7 (41,2%), мужчин – 10 (58,8%). Средний возраст пациентов – 59,7±6,9 лет. У 12 пациентов (70,5%) был инсульт по ишемическому типу, у 5 (29,5%) – по геморрагическому, средняя давность заболевания – 5,8±2,1 месяцев. 3 человека (17,6%) проживали в Москве и Московской области, 14 (82,4%) – в иных регионах Российской Федерации. Эпизодически до начала заболевания пользовались компьютером 5 пациентов или их родственников (29,4%), регулярно – 2 (11,8%), практически или никогда не пользовались – 10 (58,8%). Для всех пациентов и ухаживающих родственников, которые не пользовались компьютером в повседневной жизни или делали это чрезвычайно редко, были проведены специальные школы, в ходе которых им были даны базовые знания по использованию устройств и запуску программы реабилитации.
В контрольную группу были включены 20 пациентов. Завершили исследование при этом всего 11 (55%) из них, так как 9 человек (45%) не смогли продолжить участие: один (11,1%) в связи с обострением сопутствующей патологии, а 8 (88,9%) перестали выходить на связь.
контрольной группе женщин было 5 (45,5%), мужчин – 6 (54,5%). Средний возраст – 61,1±7,3 лет. У 7 пациентов (63,6%) был инсульт по ишемическому типу, у 4 (36,4%) – по геморрагическому, средняя давность заболевания – 6,4±2,7 месяцев. В Москве и Московской области проживали 2 человека (18,2%), в иных регионах Российской Федерации – 9 (81,8%). Эпизодически до начала заболевания пользовались компьютером 3 пациентов или их родственников (27,3%), регулярно – 1 (9,1%), практически или никогда не пользовались – 7 (63,6%). Для тех, у кого отмечались трудности при использовании компьютера, также были проведены специальные школы.
Диаграммы, показывающие состояние двигательных функций пациентов обеих групп по ИМР, представлены ниже (рис.1-2).
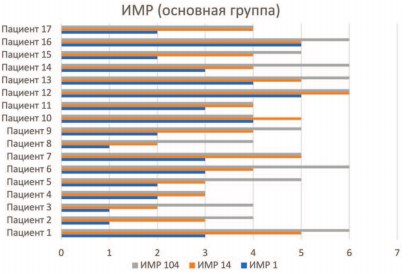
Рис. 1. Состояние двигательных функций по ИМР в основной группе на 1, 14 и 104 день.
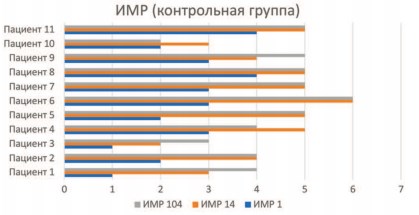
Рис. 2. Состояние двигательных функций по ИМР в контрольной группе на 1, 14 и 104 день.
Как можно увидеть на приведённых диаграммах, состояние двигательной сферы пациентов из основной группы в большинстве случаев прогрессивно улучшалось, наблюдалась статистически значимые (p<0,05) изменения как после прохождения стационарной реабилитации, так и после занятий дома. В то же время, пациенты из контрольной группы подобных результатов не продемонстрировали. С одной стороны, отмечалось статистически значимое (p<0,05) улучшение в сфере двигательных функций после прохождения реабилитации в стационаре, но при этом чрезвычайно малое количество пациентов продемонстрировало положительную динамику при повторной госпитализации после периода нахождения дома.
Динамика состояния когнитивных функций по МоСА и ОКС продемонстрирована на рисунках 3-6.
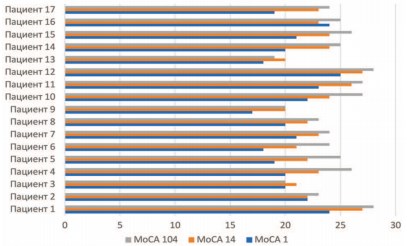
Рис. 3. Состояние когнитивных функций по МоСА в основной группе на 1, 14 и 104 день
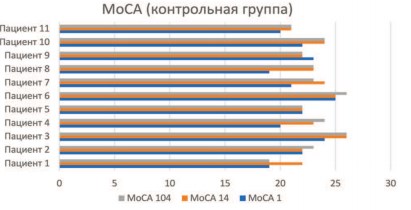
Рис. 4. Состояние когнитивных функций по МоСА в контрольной группе на 1, 14 и 104 день
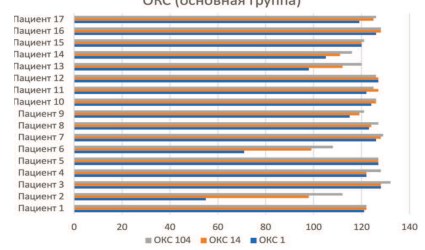
Рис. 5. Состояние когнитивных функций по ОКС в основной группе на 1, 14 и 104 день.
Можно увидеть, что в отношении когнитивных функций сохраняется схожая тенденция. Пациенты из основной группы демонстрируют значимые (p<0,05) изменения последовательно – как на этапе стационарной, так и на этапе домашней реабилитации. В то же время пациенты из контрольной группы показывают значимые (p<0,05) изменения лишь после пребывания в стационаре.
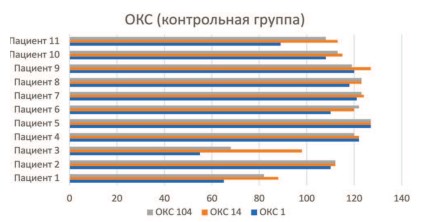
Рис. 6. Состояние когнитивных функций по ОКС в контрольной группе на 1, 14 и 104 день
Как было отмечено ранее, в отношении как двигательных, так и когнитивных функций отмечаются схожие тенденции. Так, пациенты из основной группы демонстрируют улучшения как после прохождения второго, так и после третьего этапа реабилитации, в то время как пациенты из контрольной группы чаще всего остаются на уровне, достигнутом в период стационарной реабилитации.
С этим, вероятно, связано несколько факторов. Во-первых, пациенты из основной группы продолжали структурированную программу домашней реабилитации, разработанную на стационарном этапе, в то время как пациенты из контрольной группы были вынуждены выстраивать схему занятий самостоятельно. Как сообщали пациенты и ухаживающие родственники из обеих групп, при возвращении домой им было трудно получить амбулаторную помощь, а услуги частнопрактикующих специалистов по двигательной и когнитивной реабилитации для большинства недоступны по финансовым причинам. Следует отметить, что пациенты в контрольной группе даже с благополучным социальным статусом и благоприятной поддержкой от родственников прекращали регулярные самостоятельные занятия в течение первых 1-2 недель после выписки из стационара, не смотря на то, что за время нахождения в стационаре данная категория пациентов проявляла достаточную активность в получении информации по дальнейшей реабилитации, посещала школы для пациентов и родственников, кто-то из родственников пациентов делал записи проводимых в стационаре упражнений.
Во-вторых, состояние пациентов из основной группы периодически контролировалось специалистами центра при помощи дистанционных консультаций. Отмечались результаты, достигнутые за прошедший период, ставились новые, актуальные для пациента задачи. Пациент получал обратную связь от уже знакомых специалистов, что, как мы предполагаем, в значительной степени улучшало и поддерживало мотивацию. При этом вопрос оценки мотивации пациента является сложным; проверка высказанной гипотезы достаточно затруднительна вследствие отсутствия инструментов для объективной оценки данного фактора. Можно также предположить, что присоединение фармакотерапии, в частности метаболического препарата церебролизин, влияет на восстановление не только двигательных, но и когнитивных и исполнительных функций, что в свою очередь отражается в мотивационном потенциале пациентов, что требует дальнейшего изучения.
Таким образом, можно дискутировать о том, что результаты пациентов из основной группы связаны с более высокой приверженностью реабилитации вследствие наличия индивидуального плана занятий, продолжающего контроля и своевременной обратной связи. Также следует отметить, что одним из препятствий, вставшим на пути реализации программы, стал достаточно низкий уровень компьютерной грамотности среди пациентов и их родственников. Нами были организованы специальные школы, где проводилось обучение базовым навыкам работы с компьютером (включение и выключение компьютера, соединение с интернетом, использование интернет-браузера и электронной почты), что позволило снизить влияние данного фактора. Столкнувшись же с техническими трудностями на месте, уже после возвращения домой, пациент или ухаживающий родственник мог связаться со специалистами отделения по телефону для решения возникших проблем. При повторной госпитализации пациенты и их родственники отмечали, что использование компьютера вызывает меньше затруднений.
ВЫВОДЫ
Применение технологий дистанционной реабилитации в сочетании с биологически активными нейропептидами, такими как церебролизин, может являться альтернативной схемой для поддержания приверженности пациентов реабилитации на амбулаторном этапе для повышения эффективности последней.
Исследование не имело спонсорской поддержки. Авторы заявляют об отсутствии конфликта интересов.
ЛИТЕРАТУРА
- Wittmann F, Held JP, Lambercy O et al. Self-directed arm therapy at home after stroke with asensor-based virtual realitytraining system.J Neuroeng Rehabil. 2016 Aug 11;13(1):75. doi: 10.1186/s12984-016-0182-1.
- Burton CR, Horne M, Woodward-Nutt K et al. What is rehabilitation potential? Development ofatheoretical model through theaccounts of healthcare professionals working in strokerehabilitation services. Disabil Rehabil. 2015;37(21):1955-60. doi: 10.3109/09638288.2014.991454.
- Askim T, Langhammer B, Ihle-Hansen H etal. Efficacyand Safety of Individualized Coaching After Stroke: the LAST Study (Life After Stroke). Stroke. 2018 Feb;49(2):426-432. doi: 10.1161/STROKEAHA.117.018827.
- Chen J,Jin W, Zhang XX etal. Telerehabilitation Approachesfor Stroke Patients: Systematic Review and Meta-analysis of Randomized Controlled Trials. J Stroke. Cerebrovasc Dis. 2015 Dec;24(12):2660-8. doi: 10.1016/j.jstrokecerebrovasdis.2015.09.014.
- Новак Э.В., Уварова О.А., Даминов В.Д. Опыт применения нейромодуляторов в раннем восстановительном периоде ишемического инсульта. Вестник восстановительной медицины. 2018;2:52-58. [Novak EV, Uvarova OA, Daminov VD. Experience in use of neuromodulators in early recovery period of ischemic stroke. Vestnik vosstanovitel noj mediciny. 2018;2:52-58. (in Russ.)].
- Виленский Б.С., Кузнецов Л.Н., Виноградов О.И. Повторное курсовое назначение Церебролизина новое направление реабилитации больных, перенесших ишемический инсульт. ÐÌÆ. 2008;12(16): 1658-1660. [Vilenskij BS, Kuznecov LN, Vinogradov OI. Repeated course of Cerebrolysin a new way for the rehabilitation after ischemic stroke. RMZH. 2008;12(16): 1658-1660. (in Russ.)].
- Chang WH, Park CH, Kim DY. Cerebrolysin combined with rehabilitation promotes motor recovery in patients with severe motor impairment after stroke. BMC Neurol. 2016 Mar 2;16:31. doi: 10.1186/s12883-016-0553-z.





































